
Tests rapides
Speed Trio FeLV/FIV/Corona
Test de détection combinée des antigènes circulants du FeLV (Feline Leukemia Virus), des anticorps dirigés contre le FIV (Feline Immunodeficieny Virus) et des anticorps anti-Corona Virus félin (FCOV) chez les chats.
Rapides et faciles à utiliser, les tests Speed Trio FeLV/FIV/Corona fournissent un résultat pour 3 maladies félines en 15 minutes seulement.
- Dépistage régulier des chats, particulièrement en cas d'exposition ou de risque de contact
- Seulement 3 gouttes d'échantillon pour détecter 3 virus félins
- Confirmation lors de suspicion clinique
Spécifications du produit
| Échantillon | Sang total avec anticoagulant, sérum ou plasma |
|---|---|
| Espèces cibles | Chats |
| Temps de manipulation | 2 minutes |
| Temps de résultat | 15 minutes |
| Stockage | Péremption longue de 24 mois à température ambiante (2°C - 30°C) |
| Présentation | Par boites de 6 tests |
Usage vétérinaire exclusif.
Pourquoi utiliser Speed Trio FeLV/FIV/Corona ?
Le FeLV et le FIV sont des rétrovirus responsables de symptômes non spécifiques et très variables chez les chats. De plus, la phase clinique est généralement précédée d'une phase aymptomatique de durée variable. Les tests biologiques sont donc indispensables au diagnostic différentiel (3). Le dépistage régulier des chats pour évaluer leur statut vis-à-vis des rétrovirus (FeLV ou FIV) est considéré comme le meilleur moyen de lutte contre ces virus (2). Selon les régions, les études montrent des prévalences comprises entre 1 et 20 %.
La recherche des antigènes viraux solubles du FeLV permet de déterminer le statut virémique de l'animal, même en cas de faible charge virale sanguine (infection précoce, virémie transitoire, infection séquestrée). Il peut cependant être négatif en cas d'infection latente.
La détection des anticorps anti-FCoV est utile pour guider les mesures de prévention et peut-être utilisée pour le contrôle du FCoV dans un environnement multi-chats. Un test anticorps FCoV positif indique que le chat a été infecté/exposé au FCoV et a developpé des antibocorps; la séroconversion se produisant généralement en 7 à 28 jours post-infection (1). Le test ne permet pas de différencier entre le FeCV et le virus responsable de la PIF et ne signifie pas nécessairement une infection active.
Quand utiliser Speed Trio FeLV/FIV/Corona ?
Speed Trio FeLV/FIV/Corona peut être utilisé :
Pour dépister les chats sains ou avec un historique inconnu avant vaccination, stérilisation, reproduction ou sur le point d'être intégrés dans un groupe et guider la séparation des infectés/non-infectés
Pour confirmer ou exclure une suspicion d'exposition ou clinique de rétrovirose
En association avec d'autres examens biologiques, pour ajouter une valeur diagnostique supplémentaire dans les cas de suspicion clinique de Péritonite Infectieuse Féline
En association avec d'autres examens (PCR, ELISA...), pour connaître le stade d'évolution des maladies rétrovirales dans le temps (latence ou infection active)
Guide d'utilisation
Pour des instructions détaillées, veuillez vous référer à la notice du produit.
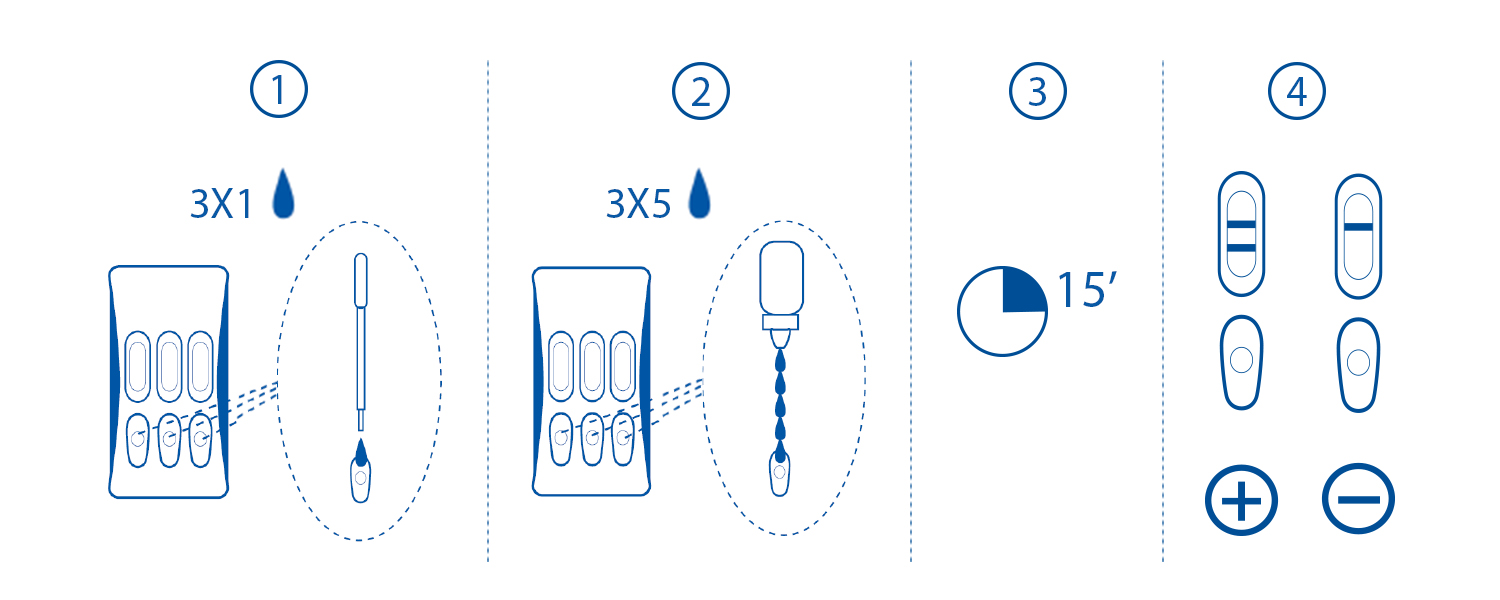
1. Ajouter 1 goutte d'échantillon dans chaque puits échantillon.
2. Ajouter 5 gouttes de réactif dans chaque puits.
3. Lecture du résultat à 15 minutes.
Performances de Speed Trio FeLV/FIV/Corona
| Méthode de référence | FeLV Viral isolation | FIV Western blot |
FCoV IFI* |
|---|---|---|---|
| Sensibilité vs ref | 94.7% | 96.3% | 96.5% |
| Specificité vs ref | 99.2% | 98.9% | 100% |
* Immunofluorescence Indirecte
Réferences
Retroviruses :
(1) HARTMANN K. et coll. Quality of different in-clinic test systems for feline immunodeficiency virus and feline leukaemia virus infection. Journal of Feline Medicine and Surgery, 2007, 9, 439-445
(2) Giselbrecht et al., Prevalence of Different Courses of Feline Leukaemia Virus Infection in Four European Countries, Viruses. 2023 Aug; 15(8): 1718.
(3) Murphy et al., The Late Asymptomatic and Terminal Immunodeficiency Phases in Experimentally FIV-Infected Cats—A Long-Term Study; Viruses. 2023 Aug; 15(8): 1775.
(4) Little, Levy et al;.2020 AAFP Feline Retrovirus Testing and Management Guidelines; J of Fel Med Surg Volume 22, Issue 1, January 2020, Pages 5-30
(5) Buch J., Beall M, o’Connor T. Worldwide clinic-based serologic survey of FIV antibody and FeLV antigen in cats. ACVIM Forum Research Abstract Program, J Vet Intern Med. 2017; 31: 1315
(6) Levy JK, Crawford PC, Tucker SJ; Performance of 4 Point-of-Care Screening Tests for Feline Leukemia Virus and Feline Immunodeficiency Virus; J Vet Intern Med 2017 Mar;31(2):521-526. doi: 10.1111/jvim.14648. Epub 2017 Feb 3.
Coronaviruses :
(1) Tasker S, Addie DD, Egberink H, Hofmann-Lehmann R, Hosie MJ, Truyen U, Belák S, Boucraut-Baralon C, Frymus T, Lloret A, Marsilio F, Pennisi MG, Thiry E, Möstl K, Hartmann K. Feline Infectious Peritonitis: European Advisory Board on Cat Diseases Guidelines. Viruses. 2023 Aug 31;15(9):1847. doi: 10.3390/v15091847. PMID: 37766254; PMCID: PMC10535984.
(2)Thayer V, Gogolski S, Felten S, Hartmann K, Kennedy M, Olah GA. 2022 AAFP/EveryCat Feline Infectious Peritonitis Diagnosis Guidelines. J Feline Med Surg. 2022 Sep;24(9):905-933. doi: 10.1177/1098612X221118761. Erratum in: J Feline Med Surg. 2022 Dec;24(12):e676. doi: 10.1177/1098612X221126448. PMID: 36002137; PMCID: PMC10812230.
(3)ADDIE D et al.. Comparison of Speed® feline coronavirus antibody rapid immunomigration tests with inderect immunofluorescence. 2008, Feline Institute Pyrenees.
(4) CACHON T., CHUZEL T. Epidémiologie, pathogénie et symptômes de la PIF. Point Vétérinaire, 2005, 254, 18-21




